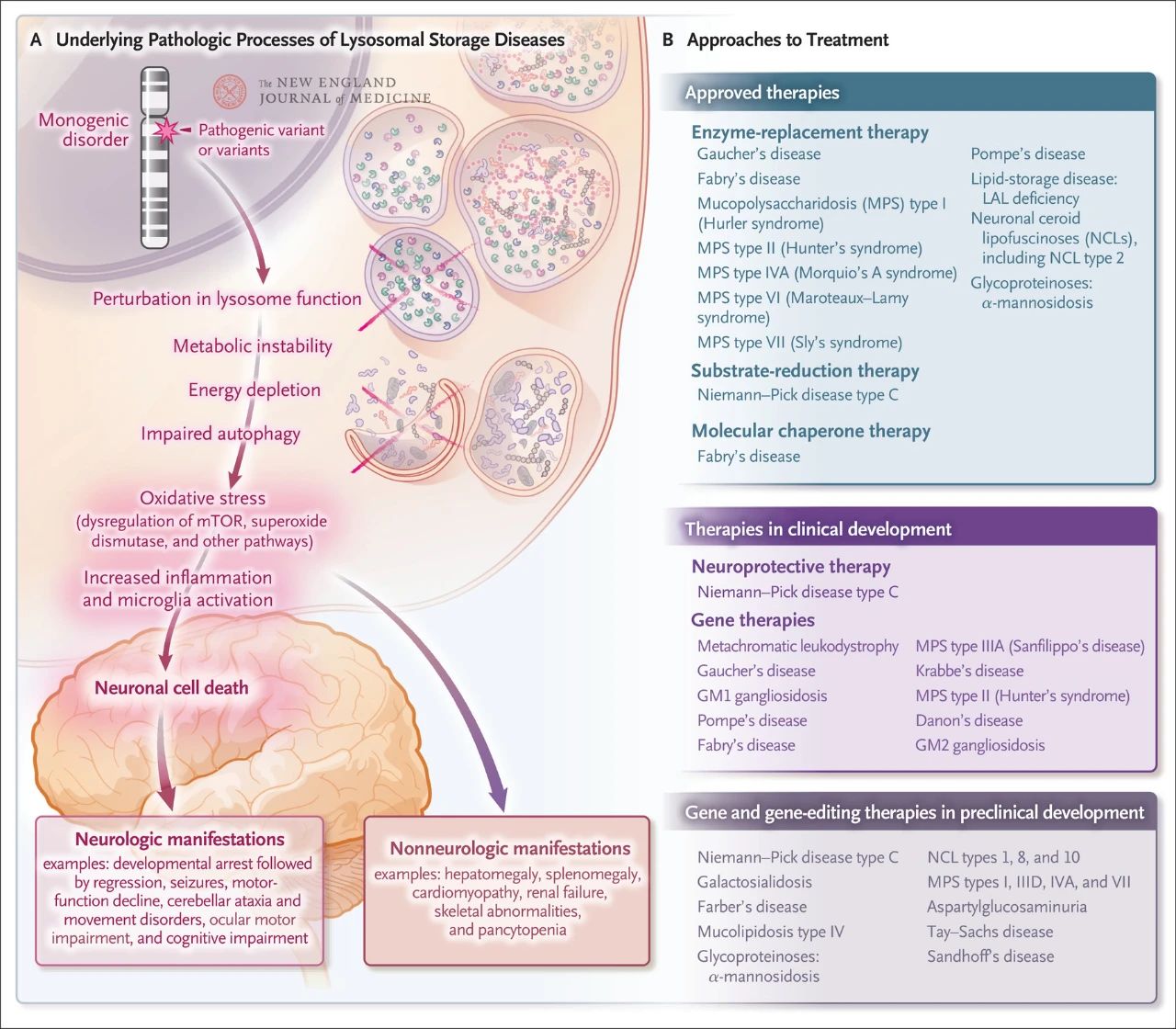
Choć stosunkowo rzadkie, łączna częstość występowania spichrzania lizosomalnego wynosi około 1 na 5000 żywych urodzeń. Ponadto, spośród prawie 70 znanych lizosomalnych chorób spichrzeniowych, 70% dotyczy ośrodkowego układu nerwowego. Te zaburzenia jednogenowe powodują dysfunkcję lizosomów, co skutkuje niestabilnością metaboliczną, dysregulacją białka docelowego rapamycyny u ssaków (mTOR, które normalnie hamuje stan zapalny), upośledzeniem autofagii i śmiercią komórek nerwowych. Zatwierdzono lub opracowano kilka terapii ukierunkowanych na podstawowe mechanizmy patologiczne lizosomalnej choroby spichrzeniowej, w tym enzymatyczną terapię zastępczą, terapię redukcją substratów, terapię chaperonem molekularnym, terapię genową, edycję genów i terapię neuroprotekcyjną.
Choroba Niemanna-Picka typu C to lizosomalne zaburzenie transportu cholesterolu w komórkach spichrzeniowych, spowodowane mutacjami biallelicznymi w genie NPC1 (95%) lub NPC2 (5%). Objawy choroby Niemanna-Picka typu C obejmują szybki, śmiertelny spadek funkcji neurologicznych w okresie niemowlęcym, natomiast postacie późnego dzieciństwa, młodzieńcze i wieku dorosłego obejmują splenomegalię, nadjądrowy paraliż wzrokowy i ataksję móżdżkową, dysartykulację oraz postępującą demencję.
W tym numerze czasopisma Bremova-Ertl i wsp. przedstawiają wyniki podwójnie ślepego, kontrolowanego placebo, badania krzyżowego. W badaniu wykorzystano potencjalny środek neuroprotekcyjny, analog aminokwasu N-acetylo-L-leucynę (NALL), w leczeniu choroby Niemanna-Picka typu C. Do badania włączono 60 objawowych pacjentów w wieku młodzieńczym i dorosłym, a wyniki wykazały istotną poprawę ogólnego wyniku (pierwotnego punktu końcowego) w Skali Oceny i Oceny Ataxii.
Badania kliniczne N-acetylo-DL-leucyny (Tanganilu), racemicznej postaci NALL i N-acetylo-D-leucyny, wydają się być w dużej mierze oparte na doświadczeniu: mechanizm działania nie został jednoznacznie wyjaśniony. N-acetylo-DL-leucyna jest zatwierdzona do leczenia ostrych zawrotów głowy od lat 50. XX wieku; modele zwierzęce sugerują, że lek działa poprzez przywrócenie równowagi między nadpolaryzacją a depolaryzacją neuronów przedsionkowych środkowych. Następnie Strupp i wsp. przedstawili wyniki krótkoterminowego badania, w którym zaobserwowali poprawę objawów u 13 pacjentów z zwyrodnieniową ataksją móżdżkową o różnej etiologii, co ponownie rozbudziło zainteresowanie tym lekiem.
Mechanizm, poprzez który n-acetylo-DL-leucyna poprawia funkcję nerwów, nie jest jeszcze jasny, ale wyniki badań w dwóch mysich modelach, jednym z chorobą Niemanna-Picka typu C, a drugim z wariantem O zaburzenia spichrzeniowego gangliozydów GM2 (chorobą Sandhoffa), inną neurodegeneracyjną chorobą lizosomalną, skłoniły do zwrócenia uwagi na NALL. W szczególności, przeżycie myszy Npc1-/- leczonych n-acetylo-DL-leucyną lub NALL (enancjomery L) uległo poprawie, podczas gdy przeżycie myszy leczonych n-acetylo-D-leucyną (enancjomery D) nie uległo poprawie, co sugeruje, że NALL jest aktywną formą leku. W podobnym badaniu nad wariantem O zaburzenia spichrzeniowego gangliozydów GM2 (Hexb-/-), n-acetylo-DL-leucyna spowodowała umiarkowane, ale istotne wydłużenie życia u myszy.
Aby zbadać mechanizm działania n-acetylo-DL-leucyny, naukowcy zbadali szlak metaboliczny leucyny, mierząc metabolity w tkankach móżdżku zwierząt z mutacją. W modelu O choroby spichrzeniowej gangliozydów GM2, n-acetylo-DL-leucyna normalizuje metabolizm glukozy i glutaminianu, zwiększa autofagię i poziom dysmutazy ponadtlenkowej (aktywnego wychwytywacza tlenu). W modelu C choroby Niemanna-Picka zaobserwowano zmiany w metabolizmie glukozy i przeciwutleniaczy oraz poprawę metabolizmu energetycznego mitochondriów. Chociaż L-leucyna jest silnym aktywatorem mTOR, nie zaobserwowano zmian w poziomie ani fosforylacji mTOR po leczeniu n-acetylo-DL-leucyną lub jej enancjomerami w żadnym z modeli mysich.
Neuroprotekcyjne działanie NALL zaobserwowano w mysim modelu uszkodzenia mózgu wywołanego uciskiem korowym. Efekty te obejmują obniżenie poziomu markerów neurozapalnych, zmniejszenie obumierania komórek kory mózgowej oraz poprawę przepływu autofagii. Po leczeniu NALL funkcje motoryczne i poznawcze u myszy z urazem zostały przywrócone, a rozmiar uszkodzenia uległ zmniejszeniu.
Reakcja zapalna ośrodkowego układu nerwowego jest cechą charakterystyczną większości neurodegeneracyjnych lizosomalnych chorób spichrzeniowych. Jeśli neurozapalenie uda się zmniejszyć za pomocą leczenia NALL, objawy kliniczne wielu, o ile nie wszystkich, neurodegeneracyjnych lizosomalnych chorób spichrzeniowych mogą ulec poprawie. Jak pokazuje niniejsze badanie, oczekuje się również synergii NALL z innymi terapiami lizosomalnych chorób spichrzeniowych.
Wiele lizosomalnych chorób spichrzeniowych jest również związanych z ataksją móżdżkową. Według międzynarodowego badania z udziałem dzieci i dorosłych z gangliozydowymi chorobami spichrzeniowymi GM2 (chorobą Taya-Sachsa i chorobą Sandhoffa), ataksja uległa zmniejszeniu, a koordynacja ruchowa precyzyjna poprawiła się po leczeniu NALL. Jednakże, duże, wieloośrodkowe, podwójnie zaślepione, randomizowane badanie kontrolowane placebo wykazało, że n-acetylo-DL-leucyna nie była klinicznie skuteczna u pacjentów z mieszaną (dziedziczną, niedziedziczną i niewyjaśnioną) ataksją móżdżkową. Odkrycie to sugeruje, że skuteczność można zaobserwować jedynie w badaniach z udziałem pacjentów z dziedziczną ataksją móżdżkową i analizowanymi powiązanymi mechanizmami działania. Ponadto, ponieważ NALL zmniejsza neurozapalenie, które może prowadzić do urazowego uszkodzenia mózgu, można rozważyć badania kliniczne z NALL w leczeniu urazowego uszkodzenia mózgu.
Czas publikacji: 02-03-2024