Hiperlipidemia mieszana charakteryzuje się podwyższonym stężeniem lipoprotein o niskiej gęstości (LDL) i lipoprotein bogatych w trójglicerydy w osoczu, co zwiększa ryzyko wystąpienia miażdżycowej choroby układu sercowo-naczyniowego u tej grupy pacjentów.
ANGPTL3 hamuje lipazę lipoproteinową i endosepiazę, a także wychwyt lipoprotein bogatych w trójglicerydy przez wątrobę. Nosiciele inaktywowanego wariantu ANGPTL3 mieli niższy poziom trójglicerydów, cholesterolu LDL, cholesterolu lipoprotein o wysokiej gęstości (HDL) i cholesterolu nie-HDL, a także niższe ryzyko miażdżycowej choroby sercowo-naczyniowej. Zodasiran to lek z grupy małych interferujących RNA (RNAi), który blokuje ekspresję ANGPTL3 w wątrobie.
Hiperlipidemia mieszana to podwyższony poziom cholesterolu LDL (lipoprotein o niskiej gęstości) i lipoprotein bogatych w trójglicerydy. Lipoproteiny bogate w trójglicerydy (w tym chylomikrony, lipoproteiny o bardzo niskiej gęstości (VLDL) i cholesterol resztkowy) odgrywają istotną rolę w rozwoju miażdżycy. Nie ma skutecznego leczenia hiperlipidemii mieszanej.
Wiadomo, że leki Batesa obniżają poziom trójglicerydów (TG), ale redukcja ta jest ograniczona. Jednocześnie leki obniżające poziom TG, w tym Bates (takie jak kwas eikozapentaenowy i octowy), nie mają istotnego wpływu na ryzyko miażdżycy spowodowanej podwyższonym poziomem cholesterolu resztkowego. Ponadto, wcześniejsze badania z udziałem pacjentów przyjmujących statyny wykazały, że skojarzone leki obniżające poziom TG nie zmniejszają ryzyka zdarzeń sercowo-naczyniowych. Czynniki te znacznie utrudniają leczenie hiperlipidemii mieszanej.
ANGPTL3 (białko podobne do angiopoetyny 3) reguluje metabolizm lipidów i lipoprotein, w tym TG i cholesterolu lipoprotein o niskiej gęstości (HDL-C), poprzez odwracalne hamowanie wychwytu lipoprotein wątrobowych zależnego od receptora lipazy lipoproteinowej, endosepizazy i lipoprotein o niskiej gęstości (LDL). Stwierdzono, że wariant inaktywacji ANGPTL3 prowadzi do zwiększonej aktywności lipazy lipoproteinowej i endosepizazy, co z kolei prowadzi do niskiego poziomu lipoprotein w osoczu w większości przypadków. Należą do nich lipoproteiny bogate w triglicerydy (tj. chylomikrony, cholesterol resztkowy, VLDL, lipoproteiny o średniej gęstości [IDL]), LDL, lipoproteiny o wysokiej gęstości (HDL), lipoproteiny (a) i ich składniki cholesterolowe. Osoby heterozygotyczne, które są nosicielami tego wariantu, mają o około 40% zmniejszone ryzyko miażdżycy, a nie zaobserwowano niekorzystnego fenotypu klinicznego. ANGPTL3 występuje w wątrobie, a terapie wyciszania genów ukierunkowane na jego mRNA, znane jako leki wykorzystujące siRNA (małe interferujące RNA), stanowią obiecującą hybrydową metodę leczenia hiperlipidemii.
12 września 2024 r. w czasopiśmie New England Journal of Medicine (NEJM) opublikowano badanie ARCHES 2, które potwierdziło, że lek siRNA zodasiran znacząco obniża poziom TG u pacjentów z hiperlipidemią mieszaną [1]. ARCHES-2 to badanie fazy 2b z podwójnie ślepą próbą, kontrolowane placebo, z eksploracją zakresu dawek. Do badania włączono łącznie 204 pacjentów z hiperlipidemią mieszaną (poziom TG na czczo 150–499 mg/dl, poziom LDL-C ≥70 mg/dl lub poziom nie-HDL-C ≥100 mg/dl). Podzielono ich na grupy otrzymujące zodasiran w dawce 50 mg, 100 mg, 200 mg oraz grupę kontrolną placebo. Pacjenci otrzymywali zastrzyki podskórne w 1. i 12. tygodniu badania, a następnie kontynuowali profilaktykę do 36. tygodnia.
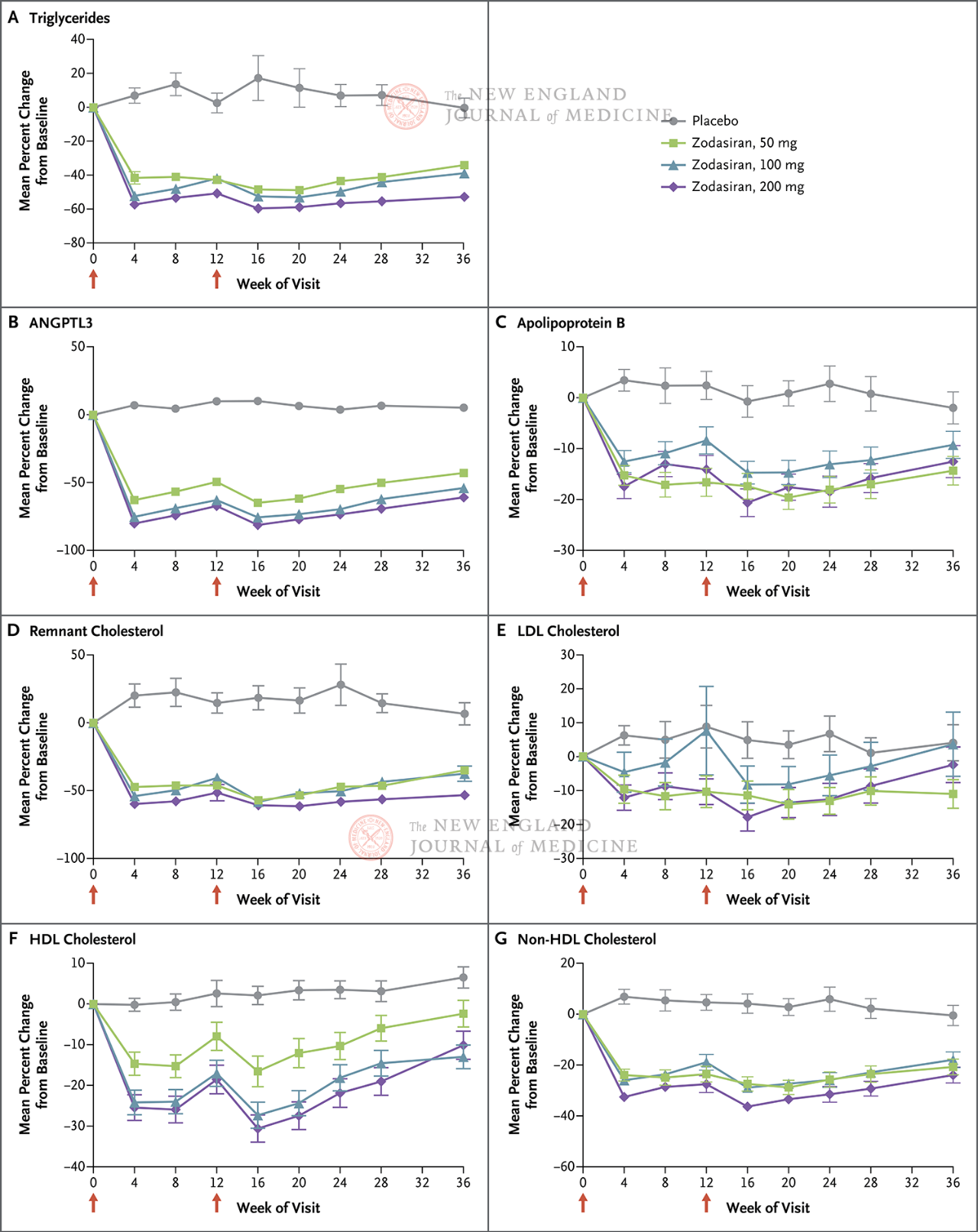
Pierwszorzędowym punktem końcowym była procentowa zmiana TG od wartości początkowej do 24. tygodnia. Badanie wykazało, że do 24. tygodnia poziomy TG w grupie zodasiran były istotnie zmniejszone w sposób zależny od dawki (poziomy TG w każdej grupie dawkowania były zmniejszone odpowiednio o 51, 57 i 63 punkty procentowe w porównaniu z grupą placebo) (P <0,001 dla wszystkich porównań). ANGPTL3 również zmniejszył się odpowiednio o 54 punkty procentowe, 70 punktów procentowych i 74 punkty procentowe. Poziomy non-hdl-c zmniejszyły się o 29 punktów procentowych, 29 punktów procentowych i 36 punktów procentowych, poziomy apolipoproteiny B zmniejszyły się o 19 punktów procentowych, 15 punktów procentowych i 22 punkty procentowe, a poziomy LDL-C zmniejszyły się odpowiednio o 16 punktów procentowych, 14 punktów procentowych i 20 punktów procentowych, a wyniki te utrzymywały się do 36. tygodnia. W 24. tygodniu zodasiran
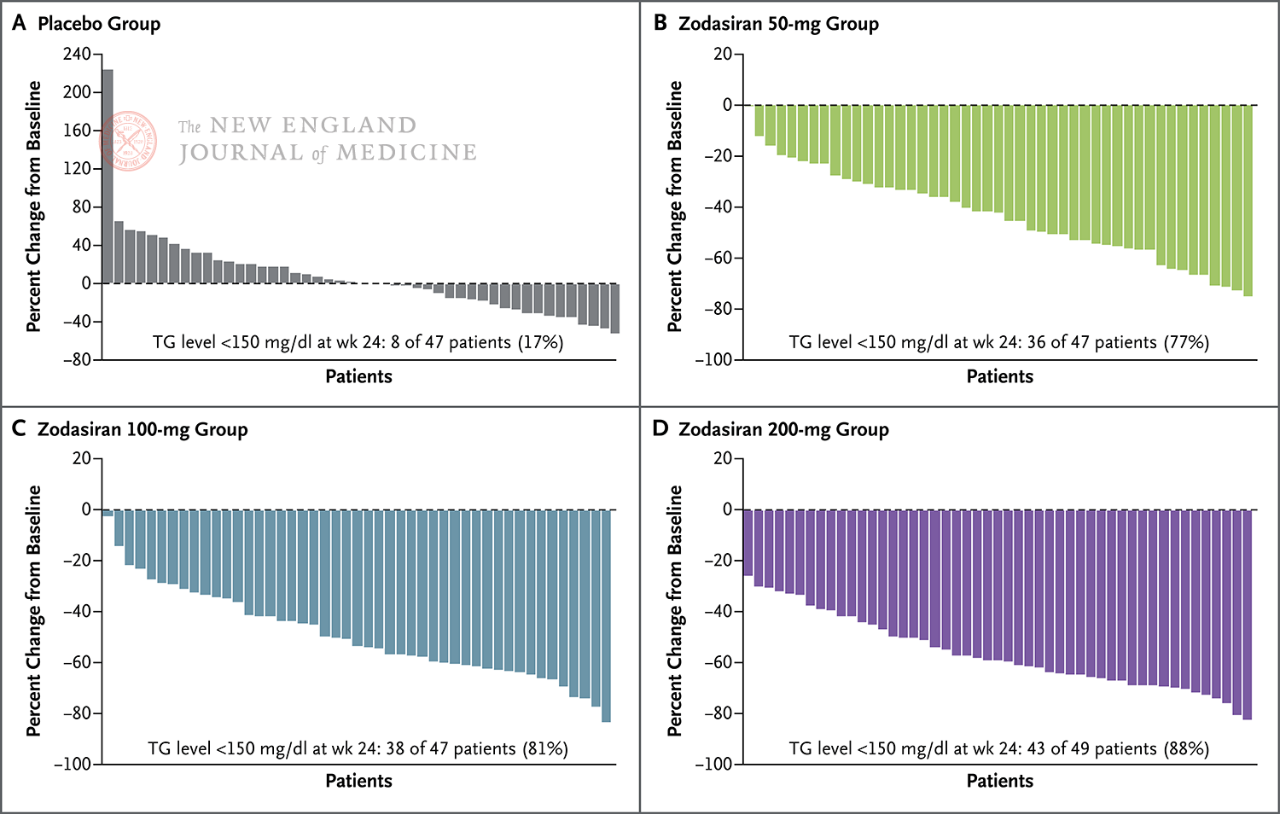
U 88% pacjentów w grupie otrzymującej 200 mg stężenie TG na czczo spadło do zakresu prawidłowego.
Czerwone strzałki w dniach 1. i 12. oznaczają podawanie zodasiranu lub placebo.
Poziomy TG na czczo spadły do normy w 24. tygodniu (150
mg/dl lub mniej)
Każdy filar reprezentuje jednego pacjenta.
W badaniu zaobserwowano również, że zotasiran był bezpieczny we wszystkich grupach dawkowania, a tylko 2 pacjentów przerwało badanie z powodu zdarzeń niepożądanych (1 w grupie placebo i 1 w grupie 100 mg zotasiranu). Wszystkie poważne zdarzenia niepożądane w grupie zotasiranu ustąpiły do końca badania, a w grupie placebo zanotowano jeden zgon. Jedynym zdarzeniem niepożądanym budzącym obawy był wzrost HBA1c w grupie 200 mg zotasiranu w porównaniu z placebo (średnia zmiana od wartości początkowej do 24. tygodnia [±SD], 0,38±0,66% w porównaniu z -0,03±0,88% u pacjentów z wcześniej istniejącą cukrzycą). U pacjentów bez cukrzycy odsetek ten wyniósł 0,12±0,19% w porównaniu z -0,03±0,19%).
W szczególności, prawie wszyscy pacjenci biorący udział w badaniu (96%) byli leczeni statynami (w tym 37% w dużych dawkach), 1% inhibitorem konwertazy proproteinowej subtylizyny 9 (PCSK9i), a 21% fibratami. Zatem dodanie zodasiranu do obecnego konwencjonalnego schematu leczenia nadal skutkowało znacznym obniżeniem stężenia lipidów, co stanowi nowy sposób leczenia hiperlipidemii mieszanej w przyszłości.
W 24. tygodniu badania maksymalna dawka 200 mg zotasiranu obniżyła poziom cholesterolu resztkowego o 34,4 mg/dl w porównaniu z placebo. Na podstawie obecnych modeli oczekuje się, że ta redukcja zmniejszy ryzyko poważnych zdarzeń niepożądanych ze strony serca o 20%. Zodasiran ma potencjał do stosowania w monoterapii wszystkich składowych lipoproteinowych w celu zmniejszenia ryzyka zdarzeń sercowo-naczyniowych u pacjentów. Konieczne są zatem dalsze badania w celu określenia potencjału tego leku w redukcji ryzyka miażdżycy.
Badanie fazy 2b, podwójnie ślepe, randomizowane, kontrolowane placebo MUIR, opublikowane jednocześnie w NEJM, wykorzystało inny lek siRNA, plozasiran, w leczeniu hiperlipidemii mieszanej [2]. plozasiran ma na celu zmniejszenie ekspresji APOC3, genu kodującego apolipoproteinę C3 (APOC3), regulator metabolizmu TG, w wątrobie, tym samym zmniejszając poziom TG i cholesterolu resztkowego. Obniżenie poziomu TG i cholesterolu resztkowego obserwowane w badaniu było podobne do obserwowanego w badaniu ARCHES-2. Dlatego też spekuluje się, że u pacjentów z hiperlipidemią mieszaną oba leki mają podobne działanie w obniżaniu poziomu lipoprotein bogatych w trójglicerydy i cholesterolu resztkowego.
Wyniki dwóch badań siRNA pokazują, że jest to bardzo obiecująca klasa leków, która otworzy nowe możliwości leczenia mieszanej hiperlipidemii i poprawi wyniki leczenia chorób układu sercowo-naczyniowego u pacjentów.
Czas publikacji: 15.09.2024